WebA first order reaction depends on the concentration of only one reactant (a unimolecular reaction ) Other reactants can be present, but their concentration has no effect on the
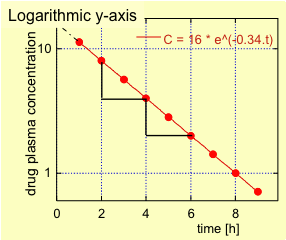
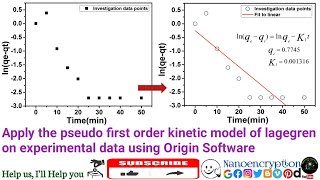
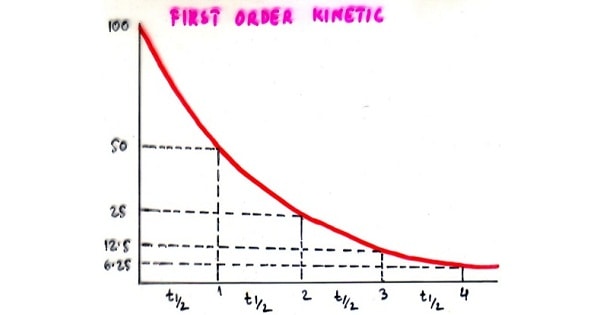
First order kinetics reaction-Web For a firstorder reaction, the concentration of the reactant decreases by a constant with each halflife and is independent of A Example The anticancer drug cisWeb Under certain conditions, the 2nd order kinetics can be approximated as firstorder kinetics These pseudo1storder reactions greatly simplify quantifying the reaction
First order kinetics reactionのギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 |  | |
 |  |  |
 |  | |
 |  |  |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |  |
 |  | |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
 |  |  |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 |  |  |
 |  |  |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  | |
 |  | |
 |  |  |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
 |  | |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 | ||
 |  |  |
 |  | |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
 |  | |
「First order kinetics reaction」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |
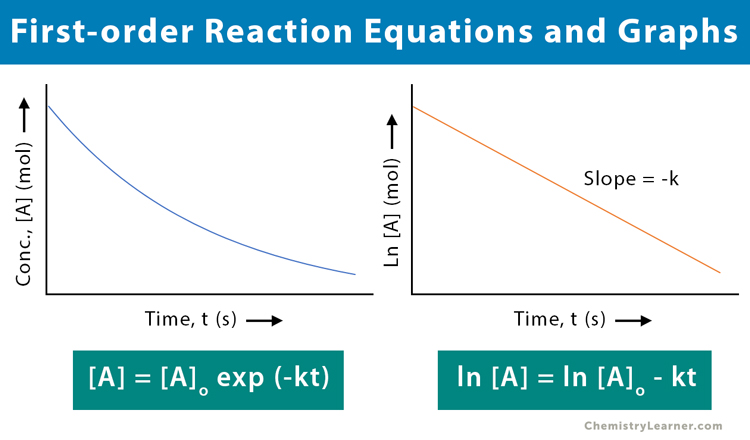
WebFirst Order Kinetics Instantaneous and Initial Rates Conic Sections Parabola and FocusWeb The differential equation describing firstorder kinetics is given below (231) R a t e = − d A d t = k A 1 = k A The "rate" is the reaction rate (in units of molar/time) and k is the reaction rate coefficient (in units of 1/time) However, the units of k vary for non
Incoming Term: first order kinetics, first order kinetics equation, first order kinetics drugs, first order kinetics formula, first order kinetics examples, first order kinetics reaction, first order kinetics graph, first order kinetics drugs examples, first order kinetics drugs mnemonic, first order kinetics pharmacology,




0 件のコメント:
コメントを投稿